FUNÇÃO ÉTER
1. Definição e Estrutura
Éteres são compostos orgânicos caracterizados pela presença de um átomo de oxigênio (O) ligado a dois radicais orgânicos (alquila ou arila).
Fórmula geral: R─O─R’
- R e R’ podem ser iguais (éter simétrico) ou diferentes (éter assimétrico).
- Exemplo: CH₃─O─CH₃ (éter dimetílico).
2. Nomenclatura
a) IUPAC (Recomendada)
- Regra: Radical menor + “oxi” + hidrocarboneto principal.
- Exemplo: CH₃─O─CH₂CH₃ → Metoxietano.
-
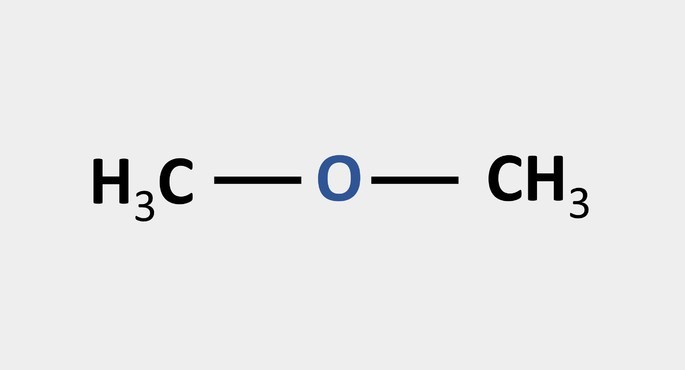
éter- função orgânica- metoximetano- imagem: Toda Matéria
b) Nomenclatura Usual (para éteres simples)
- Nome dos dois radicais + “éter”.
- Exemplo: CH₃─O─C₂H₅ → Etil metil éter.
Casos Especiais:
- Éteres cíclicos: Nomeados como óxidos.
- Exemplo: Tetraidrofurano (THF) – um solvente importante.
-
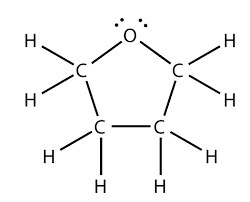
Tetrahidrofurano ( THF) – imagem: www.reeatharva.com/tetrahydrofuran
3. Principais Éteres e Aplicações
| Éter | Fórmula | Usos Principais |
|---|---|---|
| Éter dietílico | (C₂H₅)₂O | – Antigo anestésico; solvente em laboratório.
|
| THF | (CH₂)₄O | – Solvente para síntese de polímeros (como Nylon). |
| Metil-terc-butil éter (MTBE) | (CH₃)₃COCH₃ | – Aditivo de gasolina (anti-knock), hoje restrito por poluição.
|
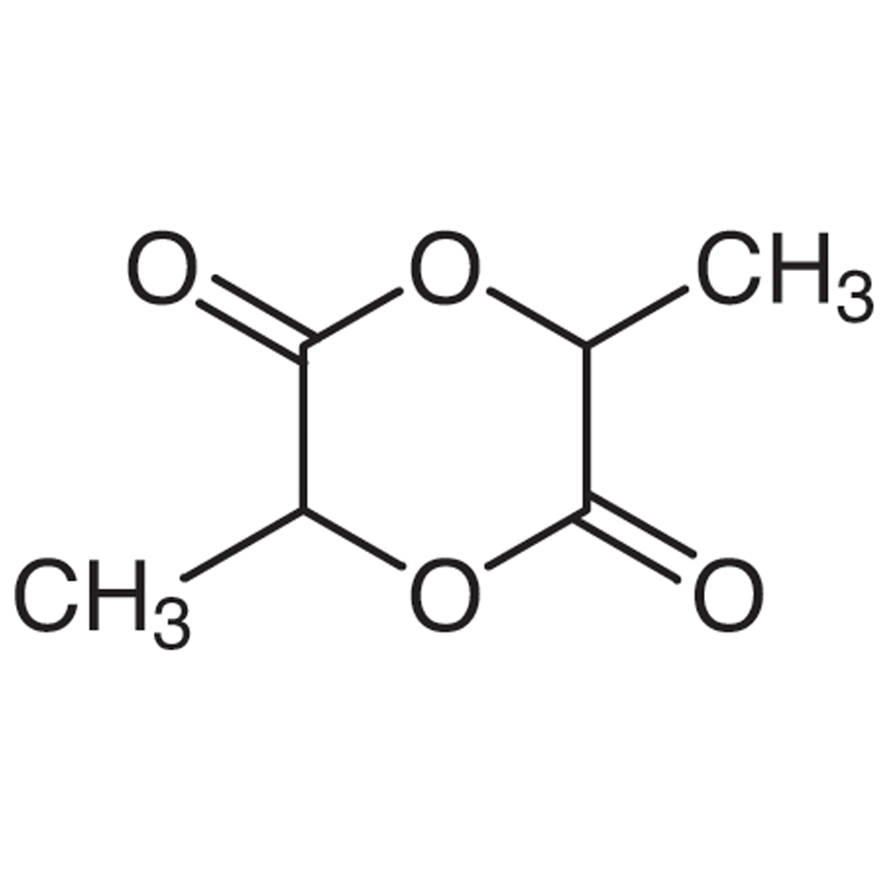
| Dioxano | C₄H₈O₂ | – Solvente industrial (resinas, tintas).
|
4. Reações Importantes
a) Formação de Éteres (Síntese)
- Desidratação de álcoois (H₂SO₄, 140°C):
- 2 CH₃CH₂OH → CH₃CH₂─O─CH₂CH₃ + H₂O
- Reação de Williamson (haleto de alquila + alcóxido):
- CH₃ONa + CH₃CH₂Br → CH₃─O─CH₂CH₃ + NaBr
b) Quebra de Éteres
- Com HX (ácidos fortes):
- R─O─R’ + HI → R─I + R’─OH (álcool).
5. Problemas e Riscos
- Inflamabilidade: Éteres como o dietílico formam misturas explosivas com o ar.
- Peróxidos: Éteres podem oxidar-se lentamente, formando peróxidos explosivos (requer armazenamento com antioxidantes).
- Toxicidade: MTBE contamina águas subterrâneas (por isso foi banido em muitos países).
6. Importância em Diferentes Áreas
- Medicina: Éter dietílico foi o primeiro anestésico cirúrgico (século XIX).
- Indústria: Solventes para extração de óleos, fabricação de plásticos (THF).
- Combustíveis: MTBE melhorava octanagem, mas foi substituído por etanol.
- Laboratório: Solventes inertes em reações (como éter de petróleo).
7. Curiosidade
O éter coroa (éteres cíclicos com múltiplos O) é usado para complexar íons metálicos, importante em catálise e química supramolecular.
8.Características físicas do éter
Quanto ao estado físico à temperatura ambiente: quando o éter apresenta de quatro a mais átomos de carbono em sua composição, apresenta-se no estado líquido;
Quanto ao ponto de fusão e ao ponto de ebulição: quando comparados com outros compostos orgânicos de massa molar aproximada, possuem ponto de fusão semelhante ao dos alcanos e menor que o restante dos compostos orgânicos;
Quanto à densidade: são compostos que apresentam uma densidade pequena quando comparados à água;
Quanto às forças de interação: os éteres são compostos com baixa polaridade, interagindo entre si por uma fraca interação dipolo permanente. Com a água e com os alcoóis, os éteres possuem a capacidade de interagir por meio de ligações de hidrogênio.
Quanto à polaridade: são compostos que apresentam geometria angular, assim, são polares.
Quanto à característica organoléptica: são substâncias que exalam um odor muito agradável, porém sua inalação pode provocar dependência.
Nomenclatura oficial do éter
Prefixo do radical menor + óxi + prefixo do radical maior + infixo + o
Para realizar a nomenclatura oficial de um éter, é fundamental determinar qual é o seu ligante maior e qual é o seu ligante menor. Para tal, acompanhe a seguir dois exemplos de aplicação para essa regra de nomenclatura:
1º Exemplo:
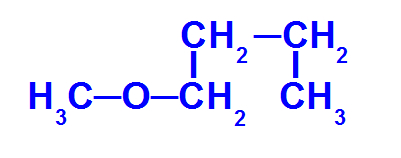
2° Exemplo:
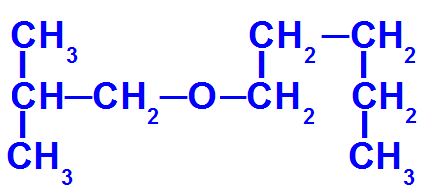
“Esse éter apresenta os seguintes radicais:
Isobutil [(CH3)2-CH-CH2-);
Pentil (CH3-CH2-CH2-CH2-CH2).
Para nomeá-lo, portanto, temos:
“prefixo do radical menor: isobut
+
oxi
+
prefixo do radical maior: pent
+
an (pois ele apresenta apena ligações simples)
+
o
Assim, o nome do éter em questão será isobutóxipentano.”
O texto do item 8- Características físicas do éter foram retirados de:https://brasilescola.uol.com.br/
SUPERINTERESSANTE -( 31/ outubro/2016)
Por que o éter, quando inalado, faz com que a pessoa desmaie?
Porque ele é capaz de “desligar” as regiões do cérebro que mantêm a pessoa consciente. Graças a essa qualidade, o éter foi um dos primeiros anestésicos ser usado no final do século passado. A substância tem a capacidade de se transformar rapidamente em vapor, indo para os pulmões junto com o ar respirado. Então passa para a corrente sanguínea e segue para o cérebro.
A partir daí a área que controla o estado de consciência é afetada e as células nervosas diminuem o envio de impulsos nervosos .
pesquisas:
Deep Seek ; brasilescola.uol.com.br ;
imagem inicial: https://lojainterprise.com.br/