A função fenol é um grupo importante na química orgânica, caracterizada pela presença de um grupo hidroxila (–OH) ligado diretamente a um anel aromático (benzeno).
Definição
Fenóis são compostos orgânicos que possuem um ou mais grupos hidroxila (–OH) ligados a um anel aromático. A estrutura básica é o benzeno com um grupo –OH, formando o fenol (C₆H₅OH).
O fenol é um sólido branco cristalino em seu estado puro. Geralmente é vendido e utilizado na forma líquida e possui odor forte, levemente doce e irritante. Apresenta diversas aplicações, como precursor ou reagente na produção de resinas, plásticos, medicamentos, herbicidas e desinfetantes.

Principais Fenóis
1-Fenol (C₆H₅OH): O mais simples e conhecido.
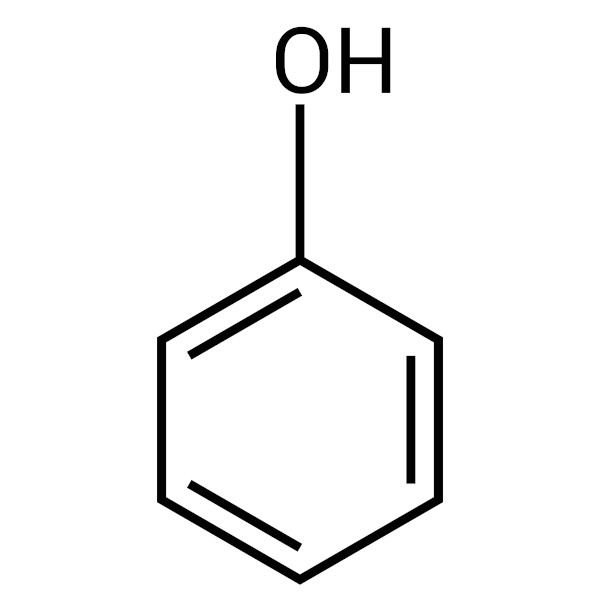
2-Cresóis (metilfenóis): Derivados do fenol com grupos metil (–CH₃) no anel aromático.
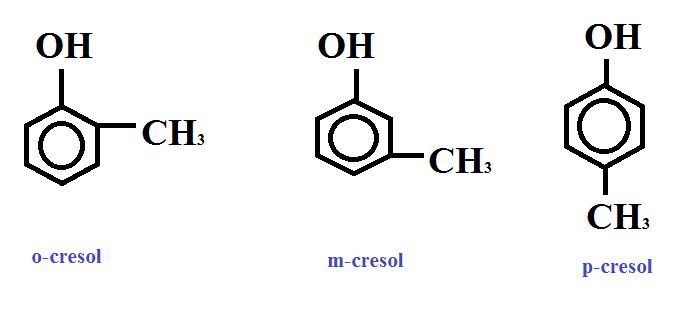
-
- Exemplos acima: orto-cresol, meta-cresol, para-cresol.
- 3- Timol: Presente no óleo de tomilho, usado como antisséptico.
-
timol- imagem: Wikipédia
- 4- Hidroquinona: Usada em produtos clareadores de pele.
-
Hidroquinona- Imagem: O Alquimista - 5- Catecol
: Presente em alguns processos biológicos.
-

catecol- imagem: Wikipedia - Ácido salicílico: Precursor da aspirina.
Utilizações
- Indústria química: Produção de resinas, plásticos (como o baquelite) e corantes.
-

baquelite- sua fórmula. O telefone visto é feito de baquelite . Imagem: PrePara ENEM - Medicina: Antissépticos, desinfetantes e fármacos (ex.: aspirina).
- O fenol e seus derivados costumam ser poderosos bactericidas porque eles têm a capacidade de coagular as proteínas dos organismos das bactérias. Por isso, o fenol comum foi muito usado como desinfetante de instrumentos cirúrgicos, o que diminuiu em muito na época o número de mortes por infecção hospitalar. No entanto, com o passar do tempo, ele foi substituído por seus derivados, porque o fenol é tóxico e corrosivo, podendo causar queimaduras.O fenol é utilizado hoje na fabricação de corantes, na preparação de resinas, na produção de fenolftaleína (um indicador ácido-base muito utilizado em processos de titulação em laboratórios), da aspirina, do ácido pícrico (que será mencionado no próximo parágrafo) e dos cresóis acima.
O 2,4,6-trinitrofenol (ácido pícrico ou picrato de butambeno) é um composto usado em pomadas para queimaduras, em detonadores de explosivos e na produção de baquelite (polímero de condensação resultante da polimerização do fenol com o formaldeído, sendo utilizado na produção de discos musicais, tomadas, interruptores, cabos de panelas, telefones, bolas de bilhar, câmeras fotográficas, revestimentos de móveis (para esta finalidade a baquelite é conhecida como fórmica), carapaças de eletrodomésticos, peças de automóveis e na produção de algumas ferramentas). ( https://mundoeducacao.uol.com.br/)
- Cosméticos: Conservantes e clareadores de pele.
- Agricultura: Produção de herbicidas e pesticidas.
- Alimentação: Conservantes (ex.: BHA e BHT).
Na natureza, os fenóis podem ser encontrados e extraídos do alcatrão de hulha, bem como também podem ser sintetizados em laboratório. Além disso, existem outros fenóis que estão presentes em vários vegetais. Alguns exemplos são:
- A carqueja é uma planta usada em chás para combater gastrite, má digestão, azia, cálculos biliares e prisão de ventre, sendo um de seus constituintes o carquejol (2-isopropenil-3-metilfenol);
- O gengibre é rico em [6]-gingerol – substância que já foi usada em testes para combater o câncer e mostrou um bom resultado;
- O eugenol é um fenol encontrado no cravo-da-índia e é usado em antissépticos bucais.
- A vanilina é a essência de baunilha obtida por meio de vagens produzidas pela orquídea Vanilla planifólia, e o timol é a essência de tomilho e é encontrado no orégano, ambos usados pela indústria alimentícia. Para saber mais, leia o texto Vanilina – Principal componente da essência de baunilha.( https://mundoeducacao.uol.com.br/)

Reações Químicas
- Eletrofilia no anel aromático: O grupo –OH ativa o anel aromático, facilitando reações como nitração, sulfonação e halogenação.
- Formação de éteres: Reação com haletos de alquila.
- Oxidação: Formação de quinonas (ex.: hidroquinona oxidada para benzoquinona).
- Esterificação: Reação com ácidos carboxílicos para formar ésteres.
Características
- Solubilidade: São solúveis em água devido à formação de pontes de hidrogênio.
- Acidez: São mais ácidos que álcoois, pois o ânion fenolato é estabilizado por ressonância.
- Odor: Muitos fenóis têm odor característico (ex.: fenol puro tem cheiro adocicado).
- Toxicidade: Podem ser tóxicos e corrosivos em altas concentrações.
Benefícios
- Antissépticos: Usados em desinfetantes e produtos de higiene.
- Fármacos: Base para medicamentos como a aspirina.
- Conservantes: Aumentam a vida útil de alimentos e produtos.
- Indústria: Essenciais na produção de polímeros e resinas.
Malefícios
- Toxicidade: Podem causar irritação na pele, mucosas e ser tóxicos se ingeridos.
- Poluição: São poluentes ambientais, difíceis de degradar.
- Carcinogenicidade: Alguns fenóis são considerados cancerígenos em exposição prolongada.
- Corrosividade: Podem corroer tecidos e materiais.
PEELING DE FENOL
Os peelings químicos são procedimentos estéticos muito procurados para rejuvenescimento facial, clareamento de manchas e tratamento de acne. No entanto, quando realizados com fenol, um composto químico poderoso, os riscos associados podem ser extremamente graves, incluindo a possibilidade de morte. Abaixo, explico os perigos e os motivos pelos quais esse procedimento pode ser fatal.

O que é o Fenol?
O fenol (C₆H₅OH) é um composto orgânico altamente ácido e corrosivo, usado em peelings profundos para remover camadas significativas da pele. Ele é eficaz no tratamento de rugas profundas, cicatrizes e manchas, mas seu uso requer extrema cautela devido à sua toxicidade.
Por que o Fenol é Perigoso?
- Toxicidade Sistêmica:
- O fenol pode ser absorvido pela pele e entrar na corrente sanguínea.
- Em altas concentrações, ele afeta órgãos vitais, como o coração, fígado e rins, podendo levar à falência múltipla de órgãos.
- Cardiotoxicidade:
- O fenol pode causar arritmias cardíacas graves, incluindo fibrilação ventricular, que pode levar à parada cardíaca e morte.
- Corrosão da Pele e Tecidos:
- O fenol é altamente corrosivo e pode causar queimaduras químicas profundas se não for aplicado corretamente.
- A aplicação em grandes áreas da pele aumenta o risco de absorção sistêmica.
- Problemas Respiratórios:
- A inalação dos vapores do fenol durante o procedimento pode causar irritação das vias respiratórias, edema pulmonar e dificuldade respiratória.
Como Pode Ocorrer a Morte?
- Absorção Excessiva:
- Se o fenol é aplicado em grandes áreas da pele ou em concentrações inadequadas, ele é rapidamente absorvido pelo corpo.
- Isso pode levar a uma overdose de fenol, causando toxicidade aguda.
- Arritmias Cardíacas:
- O fenol interfere no funcionamento do coração, podendo causar batimentos irregulares e parada cardíaca.
- Falência de Órgãos:
- A exposição ao fenol em níveis tóxicos pode danificar o fígado, rins e sistema nervoso central, levando ao colapso do organismo.
Medidas de Segurança
Para minimizar os riscos, o peeling com fenol deve:
- Ser realizado apenas por profissionais qualificados e experientes.
- Ser aplicado em pequenas áreas de cada vez, para evitar absorção excessiva.
- Incluir monitoramento cardíaco durante e após o procedimento.
- Ser evitado em pacientes com histórico de problemas cardíacos, hepáticos ou renais.
Conclusão
Embora os peelings com fenol possam oferecer resultados impressionantes, os riscos associados são significativos e podem ser fatais. A escolha de um profissional qualificado e a conscientização sobre os perigos são essenciais para garantir a segurança durante o procedimento. Alternativas menos agressivas, como peelings com ácidos mais suaves (ex.: ácido glicólico ou salicílico), devem ser consideradas para reduzir os riscos à saúde.
Imagem inicial- Portal Agro Energia
textos= DeepSeek


