QUÍMICA ORGÂNICA
A Química Orgânica é a área da química que estuda os compostos baseados principalmente no elemento carbono, incluindo suas propriedades, estruturas, reações e aplicações. Esses compostos frequentemente contêm outros elementos, como hidrogênio, oxigênio, nitrogênio, enxofre, fósforo e halogênios (flúor, cloro, bromo e iodo). A Química Orgânica é essencial para compreender os processos vitais, pois forma a base da bioquímica e está intimamente ligada à química de materiais, medicina, indústria petroquímica e tecnologia de alimentos.
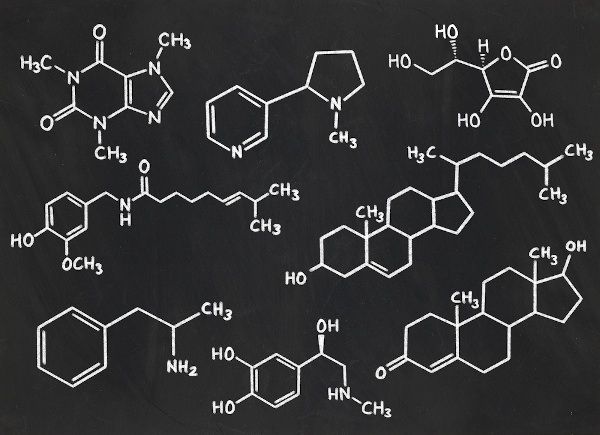
Essa área inclui o estudo de:
- Moléculas naturais (como carboidratos, proteínas, lipídios e ácidos nucleicos);
- Compostos sintéticos (como plásticos, fármacos e corantes);
- Hidrocarbonetos e seus derivados (como álcoois, ésteres e cetonas);
- Mecanismos de reação que explicam a dinâmica e os resultados das interações químicas.
Princípios Básicos da Química Orgânica
- Natureza do Carbono:
- O carbono possui quatro elétrons de valência, permitindo a formação de até quatro ligações covalentes estáveis.
-
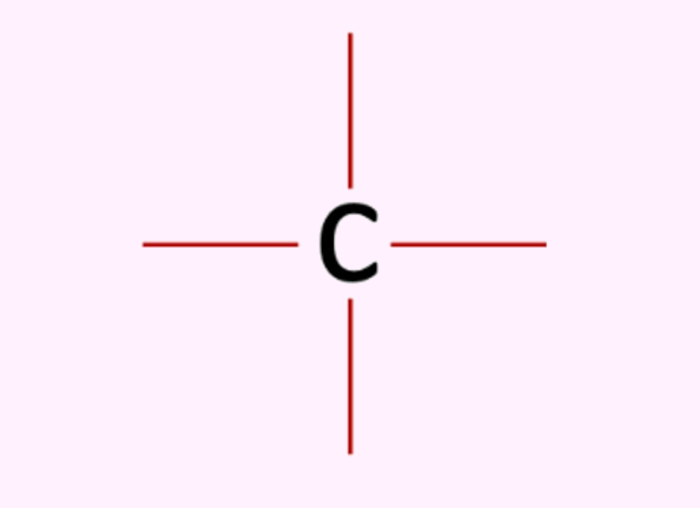
o carbono tem 4 ligações disponíveis- imagem: Mundo Educação - É capaz de formar cadeias lineares, ramificadas e cíclicas, além de ligações simples, duplas e triplas.
-
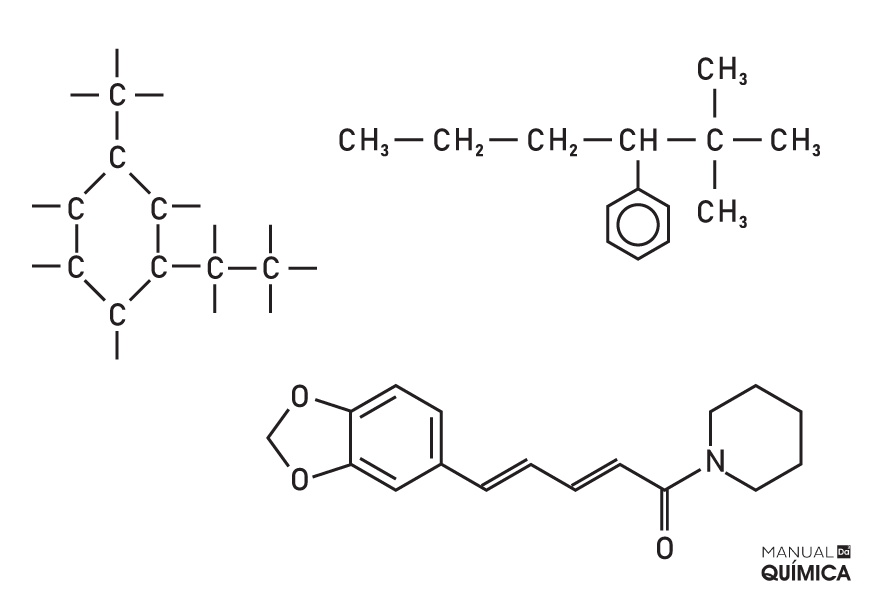
as cadeias carbônicas podem ser abertas, fechadas, mistas, envolvendo outros elementos. Imagem: Manual da Química - A capacidade de formar ligações com outros átomos de carbono (propriedade chamada catenização) é a base para a complexidade dos compostos orgânicos.
-
as quatro ligações do carbono. Ele tem a propriedade de ligar-se a outros carbonos, formando infinitos tipos de cadeias. Imagem: Conhecimento Científico
- Classificação dos Compostos Orgânicos: (cada um dessas funções será estudada separadamente)
- Hidrocarbonetos: Compostos formados apenas por carbono e hidrogênio, como alcenos, alcinos e aromáticos.
- Grupos Funcionais: Átomos ou conjuntos de átomos que definem a reatividade química de uma molécula (ex.: hidroxila, carbonila, carboxila).
- Derivados Halogenados, Ácidos Carboxílicos, Ésteres, Éteres, Amidas, entre outros.
- Ligação Química:
- As moléculas orgânicas são baseadas predominantemente em ligações covalentes.
- Interações intermoleculares, como forças de Van der Waals, ligações de hidrogênio e interações dipolo-dipolo, influenciam as propriedades físicas, como ponto de fusão e ebulição.
- Isomeria:
- Compostos com a mesma fórmula molecular podem diferir em estrutura (isomeria estrutural) ou arranjo espacial (isomeria espacial, como cis-trans e óptica).
- Reações Orgânicas:
- Classificam-se em adição, substituição, eliminação e rearranjos.
- São frequentemente descritas em termos de mecanismos de reação, que detalham a sequência de etapas intermediárias.
- Regra da Tetravalência do Carbono:
- O carbono forma sempre quatro ligações covalentes, sejam elas simples, duplas ou triplas.
-

os tipos de ligações que o carbono faz: simples, duplas ou triplas ligações com ele mesmo, ou com outro elemento. imagem:Curso Enem Gratuito
- Polaridade e Solubilidade:
- A polaridade dos compostos orgânicos depende dos grupos funcionais presentes e influencia propriedades como solubilidade em água ou solventes apolares.
- Tipos de fórmulas :
-
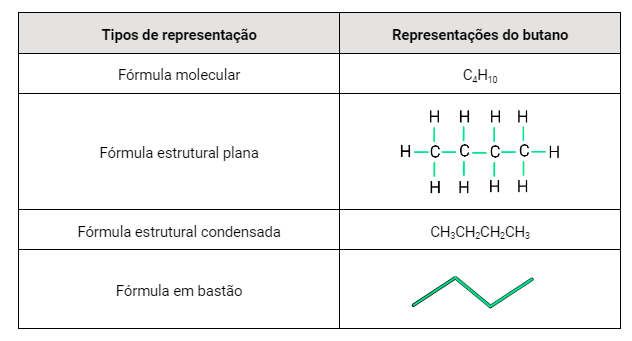
os tipos de fórmulas: molecular ( elementos e as quantidades deles na fórmula) estrutural plana ( mostrando as ligações) e a fórmula simplifica em bastão, onde cada ponta é um carbono, cada bastão, uma ligação simples. Imagem: Descomplica Exercícios

