ALÔ PESSOAL!!!
Entre as muitas teorias que são elaboradas para explicar os mais diversos fenômenos, essa tem uma importância peculiar.
Lavoisier, inconformado com essa explicação, fez seus mais brilhantes experimentos e “descobriu” o Oxigênio, que mudou todo o rumo da Química, no século do Iluminismo.
“Durante muito tempo o mistério da origem do fogo foi objeto de especulação filosófica. Várias teorias surgiram para explicar o que ocorre com os materiais no momento em que entram em combustão.
Uma delas foi desenvolvida pelo químico alemão Georg Ernst Stahl (1660-1734). Ao ler um livro de Johann Joachim Becher (1635-1682), publicado em Viena, em 1667, com o título “Physica subterranea”,algo lhe chamou a atenção. Neste livro, Becher apresentou sua própria teoria dos elementos. Segundo ele todas as substâncias eram compostas de três tipos de terras. Uma delas era a terra pinguis (literalmente, “terra gorda”), que dava à substância qualidades oleosas e a propriedade de ser combustível. Ou seja, para exemplificar, pense em uma madeira que é queimada. No inicio ela era composta de cinzas e terra pinguis, no final da combustão ela liberava a terra e permaneciam apenas as cinzas.
Ao ler este livro, Stahl, deu à terra pinguis um novo nome: “flogístico”; de origem grega “phlogios”, que significa “ígneo”. Então, ele criou uma nova teoria: a “teoria do flogístico”; e segundo ela os materiais combustíveis, como papel, madeira, enxofre, carvão e óleos vegetais, possuíam um princípio comum inflamável presente apenas nos materiais combustíveis. Se algum material não queimasse, é porque não teria flogístico em sua composição.
Esta teoria permaneceu satisfatória por muito tempo porque explicava vários dos maiores mistérios das transformações dos materiais. Além de explicar fenômenos envolvendo a combustão, englobava também os referentes à oxidação. Vejamos dois deles:
* Sem ar a combustão não ocorre– Segundo Stahl, o flogístico precisa sair para o ar durante a combustão. Mas, certa quantidade de ar só encerra uma parte de flogístico; assim, se retirássemos o ar do sistema a combustão cessaria porque o flogístico não teria para onde ir. Exemplo: se colocarmos um copo sobre uma vela acesa, ela apagará. Além disso, ele indicou o ar como imprescindível na combustão porque seria ele que transportaria o flogístico de um corpo para outro.
* Os metais aumentam sua massa depois da queima, de sua corrosão ou enferrujamento, isto é, sua oxidação – O flogístico era repelido pela terra, assim quanto mais flogístico um material possuísse, mais leve ele seria. Por isso, ao sofrer combustão o metal ficava mais pesado. Outro ponto que apoiava sua ideia era o fato de o óxido ter maior massa que o metal; desse modo, ele concluiu que o metal possuía mais flogístico que o óxido.
No entanto, esta teoria foi abandonada, pois alguns fatores entraram em contradição coma sua explicação. Por exemplo, o papel ficava com menor massa depois que era queimado, ao contrário do metal.
Um ponto culminante para a queda desta teoria foi o fato de que no século XVIII, Antoine Laurent Lavoisier (1743-1794) descobrir, por meio de inúmeras experiências bem elaboradas e controladas, a importância de um elemento químico no processo da combustão. Este elemento era o oxigênio (O). Foi desse modo que a teoria do flogístico foi abandonada.” ( Jennifer Fogaça)
Experiência de Lavoisier:
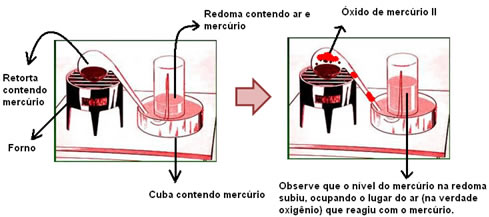
Um de seus experimentos mais famosos consistiu em colocar, em uma retorta, uma amostra cuidadosamente pesada de mercúrio metálico e introduzir o tubo da retorta em uma redoma ou cuba de vidro contendo ar e também mercúrio em sua base.
Ele aqueceu essa retorta com mercúrio por meio de um forno, causando sua calcinação. Lavoisier observou que à medida que a reação ia ocorrendo, formava-se nas paredes da retorta um pó vermelho, o óxido de mercúrio II, e ao mesmo tempo o volume do mercúrio na cuba ia subindo. Isso significava que o volume de ar estava diminuindo, pois ele estava sendo substituído pelo mercúrio, conforme pode ser visto na figura abaixo. Ao pesar o sistema inicial e o final, Lavoisier viu que a massa não havia mudado.
Assim, Lavoisier concluiu que a combustão não ocorria por causa da presença de um flogístico misterioso, mas sim porque o mercúrio ou qualquer outro material combustível reagia com outro elemento presente no ar.
Por exemplo, ele colocou uma cuba de vidro sobre uma vela acesa em uma boia com água. Ele notou que à medida que a vela ia se apagando, a água subia. E quando a água atingia um quinto do volume, a vela apagava totalmente. A conclusão foi a seguinte:
(1º) A água subia porque a vela estava consumindo o ar;
(2º) O “ar” não era o ar atmosférico todo, mas sim a quinta parte dele.
Assim, Lavoisier descobriu que esse ar estava misturado com todo o ar atmosférico e que ele era necessário para a combustão; sem ele a combustão não ocorria.

Lavoisier foi até mesmo o primeiro a fazer uma determinação experimental da composição do ar, chegando ao resultado de 21% de oxigênio e 79% de outro componente, que ele chamou de azoto, um “tipo de ar” que não participava na combustão. Hoje sabemos que se tratava do gás nitrogênio.
Inicialmente ele chamou o “ar” de “ar respirável” e depois mudou para “ar vital”. Somente em 1778 é que Lavoisier decidiu batizar o “ar vital” de oxigênio (palavra que vem do grego oxy, que significa “ácido”; e gen, “gerador ou produto”). Ele deu esse nome porque até então seus experimentos o haviam levado à conclusão de que esse novo gás estava presente em todos os ácidos; o que depois se comprovou ser uma conclusão errada, mesmo assim o nome permaneceu.
Até então o oxigênio não era considerado como um elemento químico, conforme conhecemos hoje, porque na época ainda não havia uma definição concisa para elemento.
( Jennifer Fogaça)