RADIOATIVIDADE
A radioatividade é um termo químico que causa muita desconfiança e pavor em muitas pessoas, isso se deve ao que ela ocasionou em certas situações como por exemplo os diversos ACIDENTES NUCLEARES, sendo os mais conhecidos : CHERNOBYL E FUKUSHIMA.


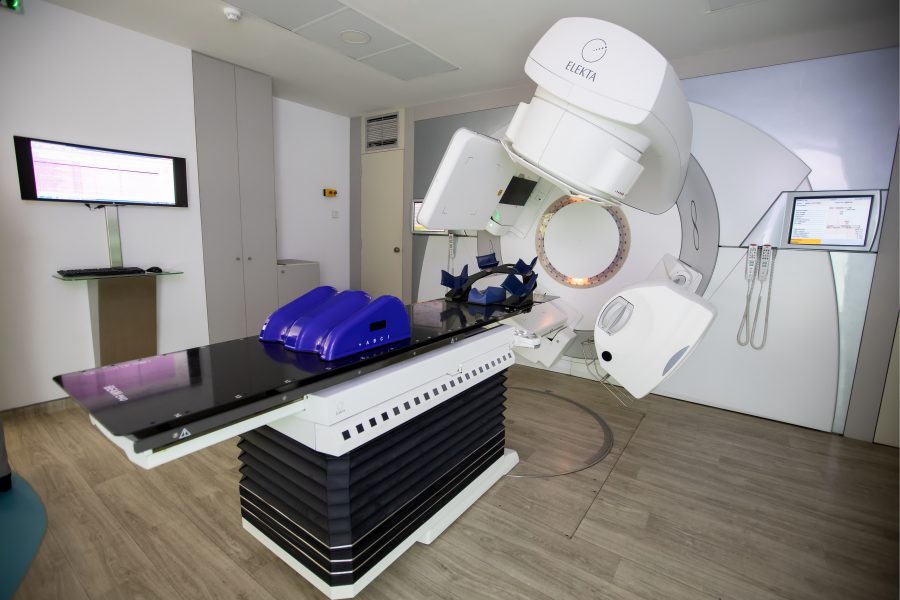
Porém, este não é um fenômeno ruim, também pelo fato de suas diversas aplicações em nosso dia a dia que possibilitaram entre outras coisas o avanço de tratamentos como o da RADIOTERAPIA.
Um elemento químico radioativo é aquele que é capaz de emitir radiações fortes a ponto de por exemplo produzir a fluorescência. O fenômeno de emissão ocorre quando o átomo se encontra com excesso de partículas e/ou cargas precisando assim liberar energia na forma de radiação para se estabilizar.
Radioatividade pode ser espontânea ou induzida, a primeira é um processo natural e e que ocorre em elementos e seus isótopos ( átomos que tem o mesmo número atômico e diferente número de massa) encontrados naturalmente, já o segundo caso se trata de um processo artificial provocado por transformações nucleares, geralmente em reatores.
As partículas emitidas por um elemento radioativo podem ser de três tipos: Alfa (α), Beta (β) e Gama (γ).
- Partícula alfa: são partículas positivas constituídas por dois prótons e dois nêutrons; não possui um alto poder de penetração. Esta partícula pode ser também chamada de núcleo de hélio (He) por ter a mesma quantidade de prótons e nêutrons deste gás nobre.
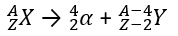
- Partícula beta: são partículas negativas constituídas por um elétron. Quando há excesso de carga negativa é liberada uma partícula beta negativa e quando há excesso de cargas positivas é liberado um pósitron ou partícula beta positiva. Seu poder penetrante é maior que o da alfa e menor que o da gama.
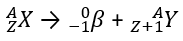
- Partícula gama: é emitida quando mesmo após a emissão das alfa e beta ainda existam cargas a serem estabilizadas no núcleo atômico, sendo esse excesso liberado em forma de ondas eletromagnéticas. Este tipo de partícula pode atingir as nossas células sendo utilizada para esterilização de equipamentos médicos por exemplo. Sua capacidade de penetração é, portanto, maior do que todas as outras formas de partículas. Esta radiação é de natureza eletromagnética e portanto, não precisa de um meio material para se propagar. Alguns tratamentos para o câncer como a teleterapia utilizam este tipo de radiação e tem como efeito a diminuição da replicação das células malignas.
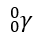
gama
CINÉTICA RADIOATIVA
Quando falamos em radioatividade, precisamos falar de cinética radioativa!
afinal, se o elemento radioativo vai emitir partículas e seu número de massa e número atômico vão mudar, então o elemento será outro!!!!
E isso acontece até que o elemento adquira estabilidade.
FATO:A cidade de Chernobyl não pode ser repopulada pelo fato de o isótopo radioativo presente no local ter uma velocidade de desintegração muito lenta.( Uranio 235 )
Quando um radionuclídeo emite partículas alfa ou beta, ele se transforma, como sabemos, em outro nuclídeo diferente. Assim, à medida que o tempo passa, a quantidade de radionuclídeo vai diminuindo.
TEMPO DE MEIA-VIDA OU PERÍODO DE SEMIDESINTEGRAÇÃO (REPRESENTADO POR T1/2 OU P) É O TEMPO NECESSÁRIO PARA QUE METADE DA QUANTIDADE DE UM RADIONUCLÍDEO PRESENTE EM UMA AMOSTRA SOFRA DECAIMENTO RADIOATIVO.

Quando a massa de um radioisótopo se reduz à metade, também se reduzem à metade o número de átomos, a quantidade em mols e a atividade radioativa (desintegrações por segundo) desse radioisótopo.
O tempo de meia-vida é uma característica de cada radionuclídeo e não depende da quantidade inicial do radionuclídeo nem de fatores como pressão, temperatura e composição química do material (lembre-se de que radioatividade é um fenômeno nuclear, e não químico).
Graficamente, podemos representar o processo de decaimento radioativo através da chamada curva exponencial de decaimento:

curva exponencial de decaimento – a cada meia vida, a massa decai pela metade, gerando a curva acima. Alfa connection
ALGUNS ELEMENTOS RADIOATIVOS E SEU TEMPO DE MEIA VIDA:

Imagine que determinado elemento possua x átomos com atividade radioativa. Após o primeiro período de meia vida, o número de átomos radioativos será de x/2. Em seguida, após o terceiro período de meia vida, o número de átomos será de x/4 e x/8 após o quarto período. Analisando a sequência: x, x/2, x/4, x/8…
Podemos concluir que o termo geral é da forma:

onde,
n = número de átomos final
n0 = número de massa inicial
x = número de períodos transcorridos ou meia vida.
Exemplo:
UM ELEMENTO QUÍMICO RADIOATIVO POSSUI HOJE 64 ÁTOMOS RADIOATIVOS. SABENDO QUE SEU PERÍODO DE MEIA-VIDA É DE 15 DIAS, QUANTOS ÁTOMOS RADIOATIVOS ELE TERÁ NO FINAL DE 3 MESES?
Solução: Temos que 3 meses = 90 dias = 6 x 15 dias = 6 períodos de meia vida. Portanto t = 6. O número de átomos radioativos hoje é de 64, portanto x = 64. Aplicando a expressão citada anteriormente, teremos:

Assim, podemos concluir que ao final de 3 meses esse elemento químico terá apenas 1 átomo radioativo.
Ou pode resolver dessa outra forma:
3 meses correspondem a 90 dias. Esses 90 dias vão dar 6 ciclos de 15 dias. Então, a cada 15 dias, perde metade da massa:
64 átomos—-> 32 átomos —> 16 ÁTOMOS —> 8 ÁTOMOS —-> 4 ÁTOMOS –—> 2 ÁTOMOS —> 1 ÁTOMO .
( CADA FLECHA VERMELHA CORRESPONDE A 15 DIAS)
EXERCÍCIOS:
1-(UESB) A radioatividade emitida por determinadas amostras de substâncias provém:
2- Relacione corretamente o tipo de emissão radioativa e suas características.
I. Emissão Alfa
II. Emissão Beta
III. Emissão Gama
a) partículas negativas, emissão em alta velocidade e poder de penetração médio.
b) partículas positivas, radiação lenta e pequeno poder de penetração.
c) ondas eletromagnéticas, não apresenta carga e possui maior poder de penetração.
RESPOSTA CORRETA: I.B; II.A E III.C.
(UEM-PR) O isótopo radioativo do iodo produzido artificialmente é usado no diagnóstico do câncer na tireóide. Quando se ingere iodo, ele fica acumulado na tireóide. Em estado normal, a glândula absorve pouco o iodo radioativo, mas, afetada pelo câncer, absorve-o em maior quantidade, podendo ser detectado por meio de detectores de radioatividade. Sabendo-se que o tempo de meia-vida do isótopo é de 8 dias, e que, após 40 dias, encontra-se uma massa de 0,5 g, qual a massa inicial do isótopo, em gramas?
RESPOSTA:
Se o tempo de meia-vida é de 8 dias, após 40 dias a massa reduziu pela metade 5 vezes, pois:
Podemos calcular a massa inicial da seguinte forma:
Onde,
- m é a massa final
- m0 é a massa inicial
- n é o número de reduções
Substituindo os valores, temos que:
Representamos as reduções segundo o tempo de meia vida da seguinte forma:
fontes:http://quimicasemsegredos.com
http:// agracadaquimica.com.br ; http://educacao.uol.com.br
fonte:https://www.infoescola.com/quimica/radioatividade
fonte: https://www.todamateria.com.br

