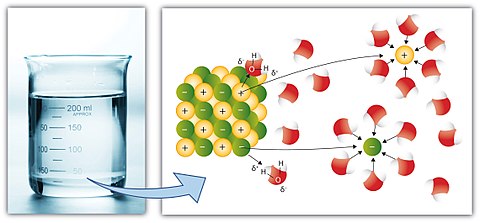
CONCEITO DE COEFICIENTE DE SOLUBILIDADE:
CADA SOLUTO POSSUI UM COEFICIENTE DE SOLUBILIDADE ESPECÍFICO, QUE É A QUANTIDADE MÁXIMA DE SOLUTO DISSOLVÍVEL EM DETERMINADA QUANTIDADE DE SOLVENTE A UMA DADA TEMPERATURA.
Mudando a quantidade de soluto, de solvente ou a temperatura, o coeficiente de solubilidade também muda.
EXEMPLO:

VEJA QUE A SOLUBILIDADE DO KNO3 AUMENTA DE ACORDO COM O AUMENTO DA TEMPERATURA.
Para o mesmo valor de água – 100g- conforme a temperatura aumenta, mais soluto se consegue dissolver.
E AÍ ENTRA OUTRO CONCEITO : SOLUÇÃO SATURADA, INSATURADA E SUPERSATURADA:
Solução insaturada
Solução insaturada é aquela que apresenta uma quantidade de soluto dissolvida menor que a especificada no coeficiente de solubilidade, ou seja, ainda é possível adicionar ao solvente uma quantidade de soluto, que será dissolvida.
Por exemplo, se o coeficiente de solubilidade do NaCl em água é de 36 g a cada 100 g de H2O, a 20 oC, temos uma SOLUÇÃO INSATURADA ( menor quantidade de soluto que o máximo possível) se prepararmos uma solução com 30 g de NaCl em 100 g de H2O, a 20 oC.
Solução saturada
Solução saturada é aquela que apresenta uma quantidade de soluto dissolvida exatamente igual à especificada no coeficiente de solubilidade, ou seja, se adicionarmos ao solvente qualquer outra quantidade extra de soluto, ela não será dissolvida.

Mas quando essa solução, com o precipitado, é aquecida, a tendência é que tudo se dissolva. Se deixarmos essa solução quietinha, ela permanece dissolvida. Mas qualquer alteração, uma batida no vidro, um cristal do soluto colocado dentro da solução, fará com que tudo que foi dissolvido em outra temperatura, retorne ao corpo de fundo.
Veja, abaixo, que as curvas de solubilidade de diversas substancias, mudam de acordo com o aumento de temperatura. Não se pode prever o comportamento de uma substancia, baseado na curva que já existe.

Exercício:
1-(Unesp-SP) A quantidade máxima de soluto que pode ser dissolvida numa quantidade padrão de solvente é denominada Coeficiente de Solubilidade. Os valores dos Coeficientes de Solubilidade do nitrato de potássio (KNO3) em função da temperatura são mostrados na tabela.

Tabela da solubilidade do KNO3
Considerando-se os dados disponíveis na tabela, a quantidade mínima de água (H2O), a 30 ºC, necessária para dissolver totalmente 6,87 g de KNO3 será de:
A) 15 G.
b) 10 g.
c) 7,5 g.
d) 3 g.
e) 1,5 g.
Resolução: Olhando a tabela: 30°C são necessários 45,8 g de soluto/ 100g de solvente
Resolução: Olhando a tabela: 30°C são necessários 45,8 g de soluto/ 100g de solvente
45,8g—————————–> 100g de água
6,87g—————————-> x X = 15 G DE KNO3
Confira o vídeo abaixo do Canal XQUIMICA :
Pesquisa: mundoeducacao.uol.com.br ,Wikipédia, Brasil escola uol .